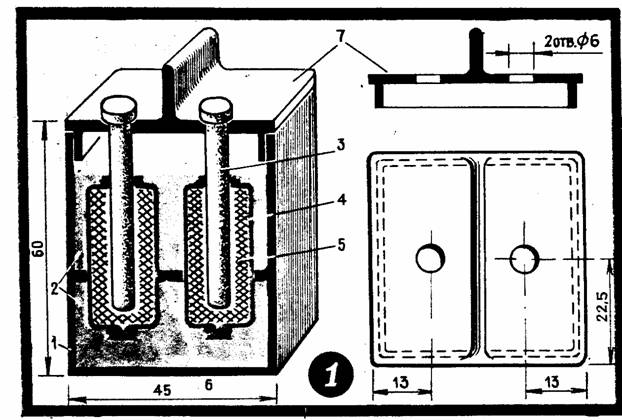
Электролизер из аккумулятора своими руками

Электролизер для автомобиля своими руками: качественное удаление ржавчины с кузова
Ионизаторы воды — бытовые электрические приборы или аксессуары, якобы способные превращать обычную водопроводную воду в минеральную. Но в отличие от природной минералки, в которой много растворенных солей, «ионизированная» вода по химическому составу практически не отличается от водопроводной. Даниил Давыдов. Все ионизаторы по принципу работы делятся на два типа: электролизные и металлические или минеральные ионизаторы. В статье мы рассмотрим оба варианта и выясним, как они работают и работают ли вообще. Интерес к водолечению возник в 19 веке.




.jpg)


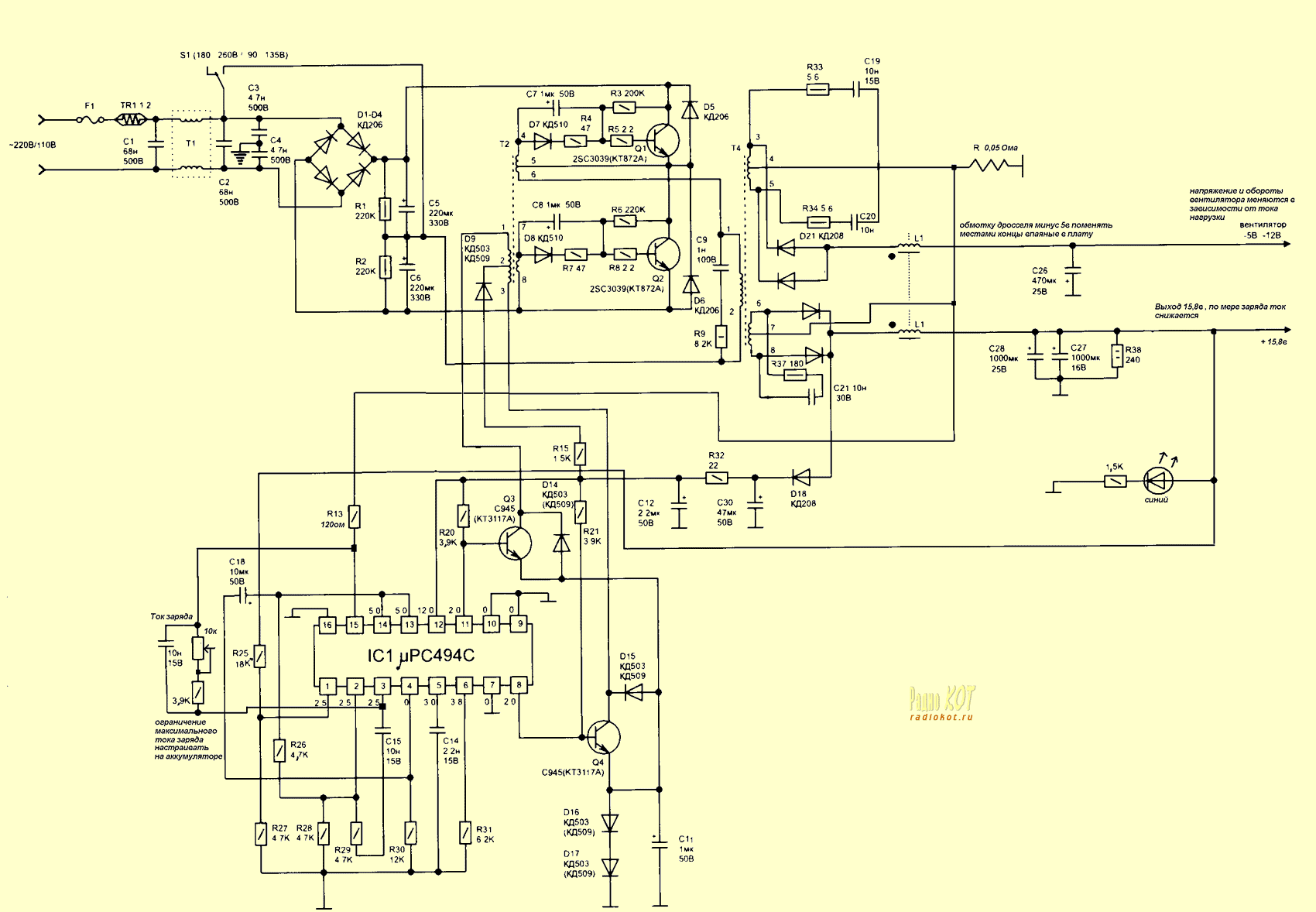
Одним из многочисленных физико-химических процессов, нашедших широкое применение, как в промышленности, так и в быту, является электролиз — выделение на поверхностях подключенных к источнику тока электродов, помещенных в раствор или расплав, их составляющих чистого металла — алюминия меди, газа и т. Основной установкой, внутри которой протекает данный процесс, является электролизер. Электролизер — это специальная установка, применяемая для выделения из раствора или расплава его составляющих. Также еще одной важной характеристикой электролизной установки является использование катализаторов.
- Эксперимент Аккумулятор своими руками | Самоделка | Дзен
- Когда я был маленький, я всё время хотел что-либо делать сам, своими рукам.
- Помогал я на днях сыну с уроками.
- Электролизер — устройство, которое применяется в производственной сфере, например, для получения определенных веществ. Однако из-за роста цены топлива и увеличения тарифов на газ ситуация в нашей стране кардинально изменилась, и теперь электролиз широко используется в домашних условиях.
- Что такое электролизер, его принцип работы, конструкция и виды
- Уменьшение мировых ресурсов природного газа заставило человечество искать другие варианты энергоносителей — недорогих, доступных и эффективных.
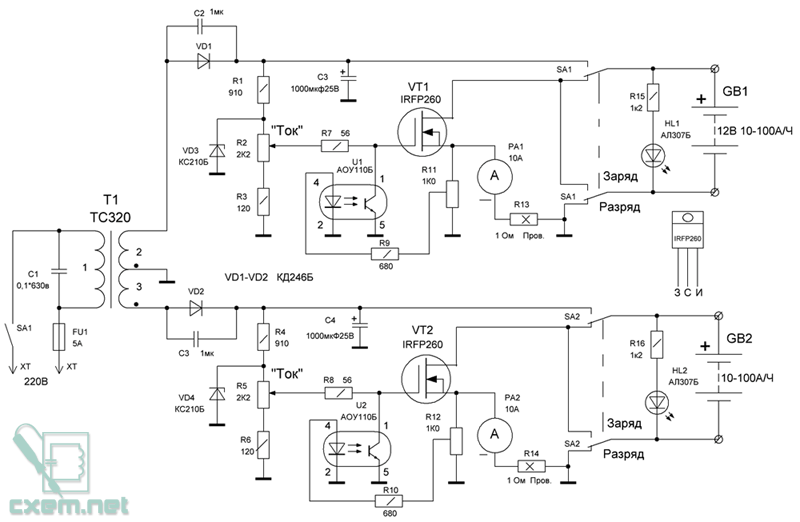
- Благодаря сотрудничеству лаборатории и организаций: Российской Железной Дороги, Речфлотом, Автотрансом, Аккумуляторными Компаниями, Минатомом и другими фирмами - разработаны ряд зарядно - восстановительных устройств, которые прошли апробирование в единичных экземплярах, даны рекомендации по эксплуатации аккумуляторов, восстановления их технических характеристик, снижения взрывоопасных выбросов водорода и кислорода, улучшение экологической обстановки и уменьшение расходов на зарядно- восстановительные работы.
- Основные области применения: стартерные аккумуляторные батареи в транспортных средствах, аварийные источники электроэнергии , резервные источники энергии. Строго говоря, аккумулятором называется один элемент аккумуляторной батареи , но в просторечии «аккумулятором» называют аккумуляторную батарею сколько бы в ней ни было элементов.






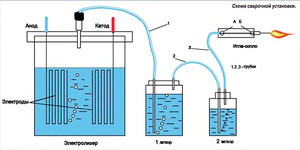
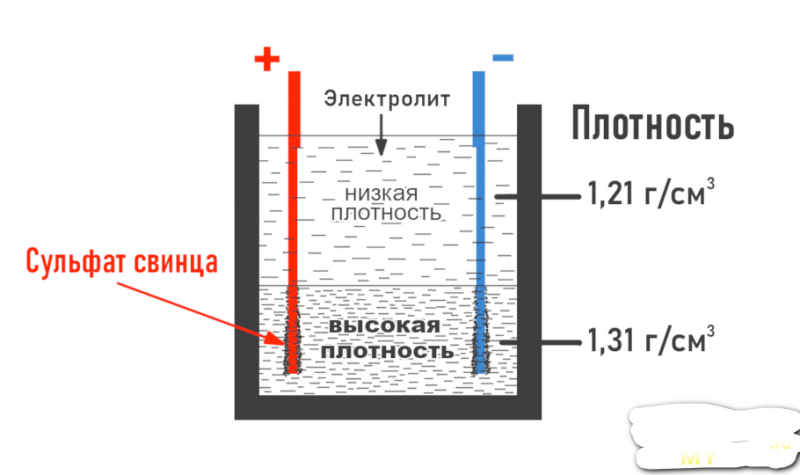
Рассмотрим окислительно-восстановительную реакцию в гальваническом элементе, тогда какие процессы протекают на его электродах? Отсюда возникает вопрос — где плюс, а где минус у батарейки? Исходя из определения, у гальванического элемента анод отдаёт электроны. В ГОСТ дано официальное определение названий выводов химических источников тока, если кратко, то плюс на катоде, а минус на аноде. В данном случае рассматривается протекание электрического тока по проводнику внешней цепи от окислителя катода к восстановителю аноду. Так как электроны в цепи текут от минуса к плюсу, а электрический ток наоборот, тогда катод — это плюс, а анод — это минус.